Dr. Stefan Lang am 13. Januar 2017
Klinische Paper schreiben: Per-Protocol oder Intention-to-treat?
In Interventionsstudien oder Wirksamkeitsstudien gibt es immer auch Probanden, die vom geplanten Behandlungsschema abweichen. Manche nehmen eine zusätzliche, nicht-erlaubte Medikation ein, andere lassen geplante Untersuchungen ausfallen oder brechen die Behandlung vollständig ab. Was geschieht mit den Daten dieser Probanden?
Es gibt zwei Möglichkeiten, in einem klinischen Paper die Daten von Probanden zu analysieren:
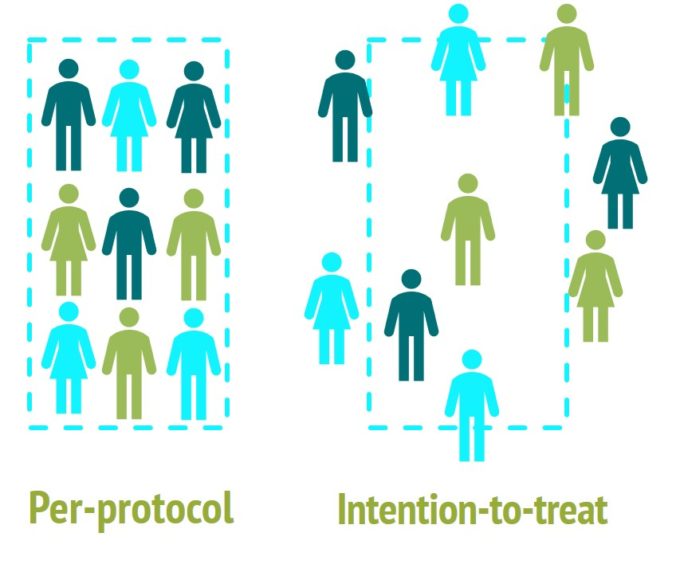
- Per-Protocol: Es werden nur die Probanden berücksichtigt, die sich zu 100% konform mit dem Studienprotokoll verhalten haben (optimale Bedingungen).
- Intention-to-treat: Es werden alle Probanden berücksichtigt, ganz gleich, ob sie vom Studienprotokoll abwichen oder nicht (Real-World-Bedingungen).
Per-Protocol-Analyse
Bei der Per-Protocol-Analyse werden ausschließlich diejenigen Probanden berücksichtigt, die sich zu 100% prüfplankonform verhalten haben. Diese Methode wählt man, wenn man in einer klinischen Studie das gesamte Wirksamkeitspotenzial einer Intervention (also eines bestimmten Medikamentes) unter optimalen Bedingungen austesten möchte.
Das sind meist Phase 1–2 Studien, in denen Verträglichkeit, pharmakologische Charakteristika, therapeutische Wirksamkeit sowie die optimale Dosis untersucht werden. Für viele andere Fragestellungen verzichten klinische Paper auf die Per-Protocol-Analyse verzichtet, denn sie hat einige gravierende Nachteile:
- Werden nicht-konforme Probanden aus der Analyse nachträglich herausgenommen, wird das Prinzip der Randomisierung verletzt. Versuchsgruppen sind unter Umständen nicht mehr vergleichbar.
- Auch ist es denkbar, dass der Grund, warum sich die Probanden nicht mehr prüfplankonform verhielten, an der Intervention selber lag, wenn etwa die Behandlung Nebenwirkungen verursachte.
- Es ist auch möglich, dass sich nur die Patienten nicht prüfplankonform verhalten konnten, die unter einer besonders schweren Form der Erkrankung litten – vielleicht waren sie zeitweise einfach nicht in der Lage, bei den Untersuchungen zu erscheinen.
Problem Per-Protocol
In den genannten Fällen können in der klinischen Publikation die Studienergebnisse verzerrt werden – meist zugunsten der untersuchten Intervention. Aus diesem Grund wird in klinischen Studien oftmals ein weiteres Datenanalyseprinzip angewandt, nämlich die Intention-to-treat-Analyse.
Intention-to-treat-Analyse
Hier werden alle Probanden, die zu Studienbeginn einer bestimmten Untersuchungsgruppe zugeteilt waren, bei der Auswertung am Studienende berücksichtigt – ganz gleich ob sie während der Studie die Behandlung absetzten, wechselten oder auf eine andere Art vom Studienprotokoll abwichen.
Das mag zunächst unlogisch erscheinen, werden doch die Behandlungseffekte unter Umständen verschleiert. Jedoch entspricht dieses Prinzip der täglichen Praxis, da in der echten Welt Patienten auch einmal ihr Medikament vergessen, versehentlich weglassen oder die Therapie wechseln (real-world patients).
Indem man alle Probanden in der abschließenden Auswertung berücksichtigt, bleibt der Stichprobenumfang groß und die Wahrscheinlichkeit verzerrter Studienergebnisse klein. Daher gilt die Intention-to-treat-Analyse auch als das Standardverfahren der klinischen Studien.
Fazit
Es gibt in klinischen Publikationen Gründe für beide Prinzipien. Beide haben Vor- und Nachteile. Während die Intention-to-treat-Anaylse die Wirksamkeit unter Real-World-Bedingungen untersucht (Effectiveness), untersucht die Per-Protocol-Anaylse die Efficacy eher im herkömmlichen Sinn. In diesem Zusammenhang könnte Sie auch der Unterschied Effectiveness versus Efficacy interessieren.

