Dr. Stefan Lang am 23. Juni 2017
Klinische Studien: Population, Sample, Study group, Dropouts
Wichtige Fragen, wenn man eine klinischen Studie in einem Originalartikel publizieren möchte: Was war die Ziel-, was war die Studienpopulation? Was waren die Einschluss- und Ausschlusskriterien und worin unterscheiden sich ‚Dropouts‘ von ‚Losses to follow-up‘?
In einem Originalartikel benutzt man für solche Dinge ein ganz bestimmtes Wording. Das sind Begriffe, die sich in der klinischen Forschung etabliert haben, die den Lesern bekannt sind. Davon sollten Sie in Ihrem Originalartikel also nicht abweichen.
Target population
In der klinischen Forschung (klinische Studie) arbeitet man mit einer relativ begrenzten Gruppe von Personen, die jedoch eine deutlich größere Gruppe repräsentieren – nämlich die Zielpopulation (target population), die zum Beispiel für eine bestimmte Behandlung prinzipiell infrage kommen. Eine Zielpopulation sind zum Beispiel alle Patienten, die an Akne leiden, 15-35 Jahre alt sind und in Deutschland leben.
Im Originalartikel schreibt man z.B.:
- target population
Study population
Es wäre natürlich unmöglich, eine Studie mit dieser gesamten Zielpopulation durchzuführen. Daher beschränkt sich die klinische Forschung auf die Studienpopulation, die die Zielpopulation bestmöglich repräsentieren soll. Das könnten etwa Patienten sein, die sich im Jahr 2016 in einer bestimmten Hautklinik wegen Akne vorgestellt haben.
Im Originalartikel schreibt man:
- study population
Sample
Oft kann jedoch auch von dieser Studienpopulation nur eine kleine Probe tatsächlich untersucht werden. Daher müssen Methoden eingesetzt werden, die eine größtmögliche Repräsentativität ermöglichen. Die Auswahl der möglichen Studienteilnehmer sollte immer zufällig und niemals systematisch erfolgen.
Manchmal werden Personen zunächst gescreent, um festzustellen, ob sie z.B. an einer bestimmten Erkrankung leiden und prinzipiell für eine Studie infrage kommen.
Im Originalartikel schreibt man z.B.:
- screened (Screening zur Vorauswahl)
- sample (Probe)
- participants (Studienteilnehmer)
Inclusion & exclusion
Wenn man aus einem größeren Personenkreis die Studienpopulation oder Stichprobe auswählt, möchte man möglichst homogene Studiengruppen untersuchen. Dafür braucht man definierte Kriterien, wer an der Studie teilnehmen darf und wer nicht: Einschluss und Ausschlusskriterien. Diese Homogenität ist wichtig, um später vergleichbare Untersuchungsgruppen zu haben und um mögliche Störfaktoren vermeiden zu können.
Einschlusskriterien beinhalten typischerweise das Alter und andere demografischen Charakteristika sowie die diagnostischen Kriterien für eine bestimmte Erkrankung.
Ausschlusskriterien regeln dagegen, welche Patienten von der Teilnahme ausgeschlossen werden, obwohl sie in der Ausgangsstichprobe waren und die Einschlusskriterien erfüllten. Gründe können zum Beispiel bestimmte Komorbiditäten sein.
Im Originalartikel:
- inclusion criteria
- exclusion criteria
Informed consent & refusals
Eine entscheidende Voraussetzung, dass Patienten an einer Studie teilnehmen können, ist die dokumentierte Einverständniserklärung des Patienten. Refusals sind die Patienten, die eine Studienteilnahme ablehnen.
- Informed consent
- Refusals
Study groups, treatment arms
In vielen Fällen wird nun die Studienpopulation mittels Randomisierung auf Behandlungsarme bzw. Studiengruppen aufgeteilt, um etwa eine Therapie vs. Placebo zu untersuchen.
Im Originalartikel:
- Randomization
- Study group, treatment arm
Dropouts & Losses to follow-up
Es kommt häufig vor, dass Teilnehmer eine Studie vorzeitig und vollständig abbrechen oder abbrechen müssen (dropouts). Die Gründe eines Studienabbruchs sind vielfältig: Wegfall eines Einschluss- bzw. Auftreten eines Ausschlusskriteriums, Nebenwirkungen, die eine weitere Behandlung unmöglich machen, Auftreten einer Begleiterkrankungen, Umzug des Teilnehmers etc.
Losses to follow-up sind Patienten einer Studie, zu denen keine vollständigen Datensätze erhoben werden konnten. Oft sind das Personen, die zwar an einer frühen Studienphase teilgenommen haben, aber zu späteren Untersuchungsterminen (follow-up) nicht mehr erschienen sind.
Die Losses to Follow-Up entsprechen also nur manchmal den Dropouts. Ist eine dieser Gruppen im Vergleich zur gesamten Studienpopulation sehr groß, führt dies unweigerlich zu Verzerrungen.
Im Originalartikel:
- Dropouts
- Losses to follow-up
- Bias (Verzerrung)
Analyzed
Am Ende ist natürlich die Zahl der Teilnehmer, die eine Studie vollständig durchliefen und ausgewertet werden konnten (analyzed), sehr viel kleiner als die Ausgangspopulation.
Eine weitere Einschränkung: Nicht alle Teilnehmer verhalten sich so, wie es in dem Prüfplan vorgesehen ist. Daher unterscheidet man bei der Analyse zwischen der per-protocol und der intention-to-treat Analyse (Link für weitere Infos).
- analyzed
- per-protocol (nur Prüfplan-konform)
- intention-to-treat (alle)
Flow & patient characteristics
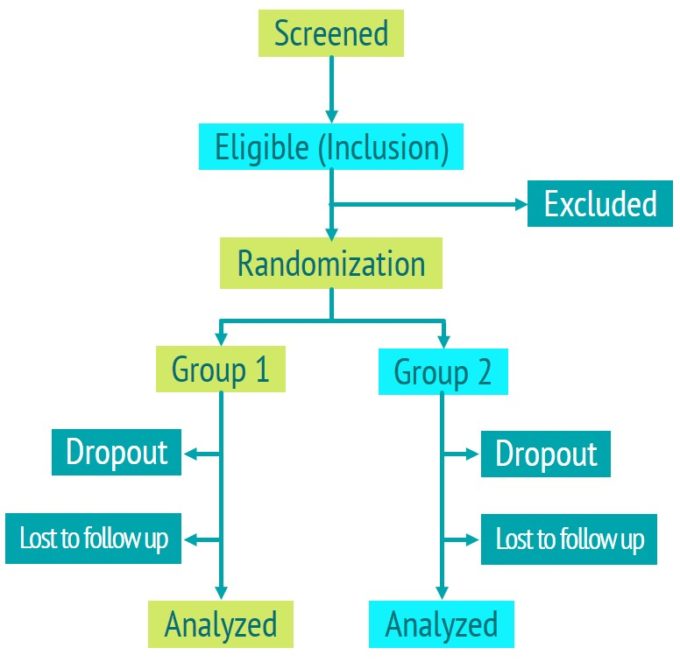
Oft wird der „Fluss“ der Teilnehmenden durch die einzelnen Auswahl- und Aufteilungsschritte in einem Flussdiagramm dargestellt (Abbildung oben). Dieser patient flow ist dann die erste Abbildung im Ergebnisteil des Originalartikels.
Anschließend wird meist die am Ende resultierende Population charakterisiert, nach Studiengruppen getrennt: patients characteristics. Das ist dann meist die erste Tabelle im Paper.
Fazit
Wichtig ist also, die richtigen Begriffe zu wählen, wenn es an die Publikation einer Studie geht. Besonders wichtig ist die Charakterisierung der Studienpopulation (Methods), die Beschreibung der Einschluss und Ausschlusskriterien (Methods) sowie ein Flussdiagramm mit den Zahlen der gescreenten, rekrutierten, ausgeschlossenen und randomisiert verteilten Teilnehmern (Results). Nicht zu vergessen sind auch der informed consent (Results) und die Nennung der Analysemethode – per protocol oder intention-to-treat? (Results).
Dr. Stefan Lang
Das Paper-Protokoll
Eine systematische Schreibanleitung für biomedizinische Originalartikel
Wenn Forscher im Labor experimentieren oder in der Klinik Daten erheben, folgen sie genauen Anleitungen, die alle Arbeitsschritte exakt definieren. Eine solches Protokoll gibt es jetzt auch fürs Schreiben und Publizieren eines Research Papers.
Das Paper-Protokoll
kaufen bei
Paperback ISBN : 978-3-7345-4167-4
Hardcover ISBN : 978-3-7345-4168-1
E-Book ISBN : 978-3-7345-4169-8




